Het beroemde gedicht van Samuel Coleridge ‘De rijpheid van de oude zeeman‘ citeerde: ‘Water, water, overal, geen druppel om te drinken!’ Via deze beroemde regels gaf Coleridge aan dat hij geen water had om te consumeren, ondanks dat hij omringd was door een oceaan. Hij vertelde ook dat hij een albatros had gedood (wat volgens de plaatselijke overlevering iedereen op het schip ongeluk brengt). Natuurlijk bevestigt hij via zijn beroemde regels ook de algemene kennis dat 75% van het aardoppervlak water bevat. Bovendien weten we ook dat 60% van het menselijk lichaam uit water bestaat. Water (een eenvoudig molecuul) blijkt dus cruciaal in alle processen.
Om studenten meer te laten leren over dit bekende fenomeen (in detail), geven scheikundedocenten huiswerk op over de chemische eigenschappen van H2O, de structuur ervan, de betekenis voor het milieu, enz. om de diepte van hun begrip te bepalen. Studenten, die niet op de hoogte zijn van de chemische eigenschappen, structuur en algemene betekenis, hebben echter vaak moeite om goed onderbouwde en unieke artikelen samen te stellen binnen de krappe deadline. Gelukkig zijn er verschillende opmerkelijke websites voor opdrachtbegeleiding (zoals TopHuiswerkHelper) bieden 360-graden huiswerkhulp over scheikunde voor zowel basis- als geavanceerde onderwerpen.
Hun op maat gemaakte begeleiding stelt studenten in staat hun onderwerp-/conceptkennis te vergroten, hun academische schrijfvaardigheid te verbeteren en inzendingswaardige papers voor te bereiden voor uitstekende cijfers. Je kunt het uitproberen als je soortgelijke problemen ondervindt bij het begrijpen van specifieke scheikundeonderwerpen die in hun curriculum zijn opgenomen.
Niettemin leggen we hieronder alles wat de titeldekking betreft helder uit om u op weg te helpen met uw huiswerk.
De chemische eigenschappen van water
Omdat het een chemische stof is, reageert (H2O) met veel stoffen om verschillende chemische verbindingen te vormen.
Redoxreactie: Als een prachtige bron van waterstof (met twee waterstofatomen die covalent gebonden zijn met één zuurstofatoom), verminderen de elektropositieve elementen waterstofmoleculen.
Tijdens fotosynthese wordt H2O gereduceerd en geoxideerd tot O2, wat van vitaal belang blijkt voor redoxreacties. (Bekijk voorbeeld)
![]()
Sfeervol van aard: Velen weten misschien dat H2O kan dienen als base en zuur. Dat geeft aan dat het van nature atmosferisch is. (Bekijk voorbeeld)
Zuur gedrag:
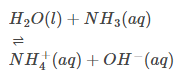
Basisgedrag:
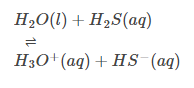 Hydrolysereactie: Het heeft ook een sterke hydraterende neiging, voornamelijk vanwege de diëlektrische constante, en kan verschillende iconische verbindingen oplossen. Bepaalde ionische en covalente verbindingen kunnen worden gehydrolyseerd.
Hydrolysereactie: Het heeft ook een sterke hydraterende neiging, voornamelijk vanwege de diëlektrische constante, en kan verschillende iconische verbindingen oplossen. Bepaalde ionische en covalente verbindingen kunnen worden gehydrolyseerd.
Zeker huiswerkbegeleiding op de universiteit van TopHomeworkHelper.com en krijg gratis toegang tot talloze scheikundige antwoordoplossingen/schrijfnotities.
Meer over H2O-eigenschappen
- Molaire massa – 8,01528(33) g/mol
- Vaste dichtheid – 0,9167 g/ml bij 0 °C
- Vloeistofdichtheid – 0,961893 g/ml bij 95 °C, 0,9970474 g/ml bij 25 °C, 0,9998396 g/ml bij 0 °C
- Smeltpunt – 0 graden C
- Kookpunt – 100 graden C
- Zuurgraad – 13.995
- Dampspanning – 0,032176 atm/3,1690 kilopascal
- Viscositeit – 0,890 cP
- Thermische geleidbaarheid –0,6065 W/m·K
- Brekingsindex – 1,3330 (nD)
- Basiciteit – 13.995 (pKb)
De chemie van de waterstructuur
De chemische structuur van water bestaat uit twee verschillende waterstofatomen die zich binden met één enkel zuurstofatoom. Vanwege de hogere elektronegativiteit van zuurstofatomen heeft het polaire covalente bindingen. Het zuurstofatoom lokt de gedeelde elektronen van de covalente bindingen in grotere mate in tegenstelling tot waterstofatomen. Daarom worden de zuurstofatomen negatief geladen (gedeeltelijk), terwijl de waterstofatomen een gedeeltelijk positieve lading ontvangen. De atomen nemen dan een gebogen structuur aan vanwege 2 eenzame elektronenparen op het zuurstofatoom. De gebogen vorm van het watermolecuul ontstaat doordat polaire O-H-bindingen elkaar niet opheffen en het hele molecuul polair is.
Bovendien trekken de polaire bindingen elkaar aan via de dipool-dipoolkrachten (het positieve uiteinde van één molecuul wordt aangetrokken door het negatieve uiteinde van het nabijgelegen molecuul). In water hebben de polaire O-H-bindingen weinig elektronendichtheid nabij de waterstofatomen, waarbij elk H2-atoom aangetrokken wordt door de eenzame elektronen op een aangrenzend O-atoom. Het wordt waterstofbruggen genoemd en ze zijn sterker dan alle normale dipool-dipoolkrachten.
Milieubelang
Nu de wereldbevolking elk jaar groeit, het belang voor het milieu en de behoefte aan bruikbaar water nemen ook toe.
Water is ook belangrijk voor het voeden, groeien en verzorgen van verschillende planten en dieren (zelfs de beweging en voortplanting van vissen). Routinematige bewateringsevenementen voor bloeiende planten bieden ook voedsel en onderdak aan insecten, reptielen, kikkers en zoogdieren. Zelfs bosvogels reageren goed op gezonde wetlands. Ze kunnen zich gemakkelijk voeden en verplaatsen om planten te bestuiven en insecten en ongedierte te reguleren.
Het publiek moet de waarde van water in grotere relevantie erkennen. Schoon water is van cruciaal belang voor de landbouw, de veehouderij, de sanitaire voorzieningen en het behoud van het omliggende ecosysteem. Water helpt de natuurlijke stroming in rivieren, wetlands, kreken, enz. te herstellen en in stand te houden en helpt habitats in uiterwaarden te ondersteunen.
Het is dus belangrijk dat de wereldregering en andere officiële instanties die verantwoordelijk zijn, een gezond, hernieuwbaar en veerkrachtig watersysteem in stand houden, in ieders voordeel.
Source: De chemie van water: eigenschappen, structuur en betekenis voor het milieu